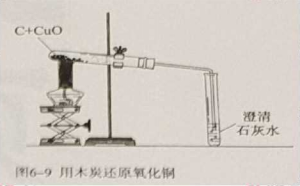
(1)黑色的粉末逐渐变为红色,且产生可以使澄清石灰水变浑浊的无色无味的气体。
(2)【教学目标】
知识与技能目标:掌握碳的化学性质;了解碳的还原性;
过程与方法目标:通过阅读,实验验证,分析对比等,掌握单质碳的化学性质:稳定性,可燃性,还原性;引导学生体会化学实验是获取化学知识和学习科学探究方法等的重要手段。
情感态度价值观目标:使学生理解结构,性质,用途三者间的辨证关系,证明实践出真知的真理性培养学生归纳整理,寻找规律的能力。
教学方法:实验探究法与思维探究法
教学过程:
(一)导入
多媒体展示水墨字画与钻石,并提出问题:古代一些书法家、画家用墨写字作画,我们知道墨的主要成分是碳黑,这些字画历经千百年,但墨迹依然清晰不变,又如由金刚石琢磨而成的钻石,经风吹,日晒,雨淋仍不发生变化。这体现了碳的哪些性质呢?导入教学内容。
(二)新授
教师提问:能否从碳原子的核外电子排布来分析为什么碳单质在常温下具有较为稳定的化学性质?
学生组内讨论,尝试从碳的原子结构推断其稳定的原因。
教师提问:木制的电线杆在埋入地下前,将其表面烧焦的目的是什么?
学生组内探讨,总结:是为了使木材表面形成焦炭,其化学性质在常温下比较稳定,不易和其它物质发生化学反应,使电线杆即使埋在地下的部分也不易腐烂。
教师引出碳的第一个化学性质——稳定性
教师提问:教师多媒体展示冬天取暖过程中煤气中毒的短视频,提出问题,上述的反应原理是什么?怎样避免上述情况的发生?
学生总结出碳在氧气充足和氧气不充足时反应的方程式,对碳的可燃性进行初步认识。并通过对预防煤气中毒的分析,让学生初步对燃料的燃烧安全有一定的认识。
【演示实验】教师演示碳还原氧化铜实验,引导学生观察实验装置、操作及实验现象。
教师引导学生回忆实验的操作步骤,并通过提问的形式对实验中需要注意的事项进行分析。实验后教师进行请学生记录实验现象,并引导学生对实验现象进行分析、归纳和总结。
教师介绍还原反应、还原性等概念,并对碳的还原性进行进一步的介绍。
教师展示单质碳在冶金工业中的应用资料卡片,辅助学生进一步理解碳的还原性应用。
(三)巩固小节
教师通过习题的方式检测学生对于本节内容的掌握情况,并请学生总结本节课的收获。
(四》布置作业
教师请学生在课后通过查询资料的形式,了解碳的化学性质的应用。