(1):1、Mg+2HCl=MgCl2+H2↑
2、Fe+2HCl=Fecl2+H2↑
(2)
—、教学目标:
1.掌握酸的化学性质。
2.进一步认识和体验科学探究的过程提升探究能力。
3.运用实验的方法获取信息,运用比较、概括等方法多获取的信息进行加工。
增强对化学现象的探究欲,培养学生共同合作、勤于思考的科学精神。
二、教学方法:实验探究法、小组讨论法、演示法、启发引导法、多媒体演示法、讲授法等。
三、教学过程
1.导入:采用联系生活的方式导入该课程。师:同学们我们在生活中、工业生产中一定听说过很多种类的酸,那么哪位同学能够告诉老师你们知道有哪些酸是我们在工业生产、生活中比较常见的。
生:硫酸、盐酸、醋酸....
师:同学们说的非常好,那么酸又具有哪些性质,又会发生怎样奇妙的化学反应呢,带着这样的问题我们进入到本节课的学习。
作用:通过该过程不单可以激发学生对于本节课的兴趣,实现课未始兴已浓的学习氛围。
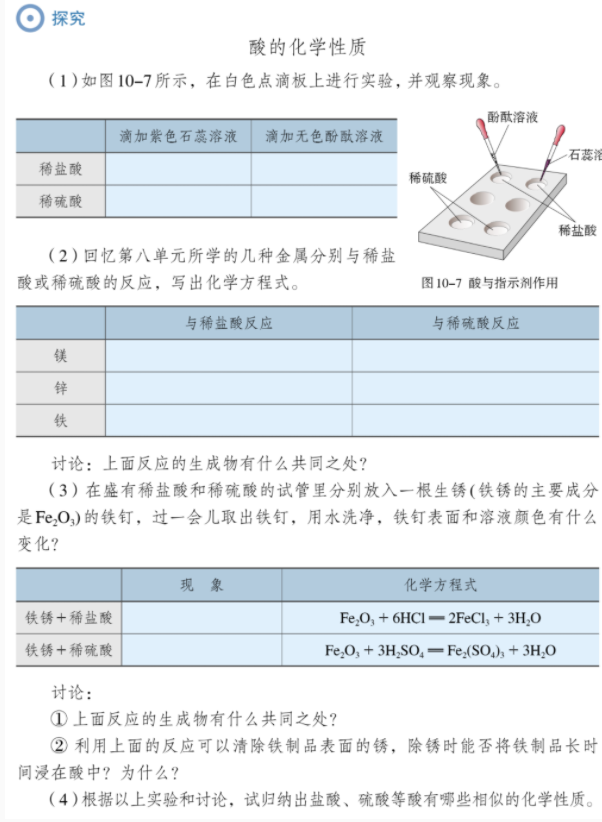
2.新授:活动一:分发白色点滴板,引导使用酸碱指示剂进行酸的滴定实验。并引导学生通过对酸碱指示剂与酸的显色反应进行记录,并采用启发引导的方式进行提问。师:各位同学哪位同学能够告诉老师,不同的酸与酸碱指示剂进行显色反应的现象。生:酸能够使酸性指示剂变红,而无法与碱性指示剂发生反应。
作用:通过该过程提升学生归纳总结的能力,并深化实验探究能力
活动二:通过多媒体演示法展示之前所学习的酸与不同金属反应,并引导学生回顾酸与金属反应的产物,并采用提问的方式引导学生在实验手册上书写化学反应方程式,并在书写过程中给予引导。在学生完成反应式书写后引导学生以实验小组讨论酸与金属反应的特征。
作用:强化获取信息,运用比较、概括等方法多获取的信息进行加工。
增强对化学现象的探究欲,培养学生共同合作、勤于思考的科学精神能力与意识。
活动三:讲解铁锈的主要成分以实验小组为单位进行实验设计,并铁钉与酸的化学反应实验,学生做好实验记录并对实验产物进行猜想。教师采用讲授的方式明确反应过程
作用:通过该过程进—步加深学生实验探究能力,强化探究意识培养学生共同合作、勤于思考的科学精神。
三、习题练习,巩固新知
设置谈论环节:以实验小组为单位讨论使用酸除锈,铁制品是否可以长时间浸泡。
四、自我总结,分享收获
由学生总结本堂课的收获,教师对学生的课堂表现予以肯定,并做情感态度的升华。
五、紧扣主题,扩展延伸
课后让学生查阅资料,查询酸在生活中的应用并思考利用了酸的哪些性质。